Pe lângă tehnologie, sinteza glicozidelor a fost întotdeauna de interes pentru știință, deoarece este o reacție foarte frecventă în natură. Lucrări recente de Schmidt, Toshima și Tatsuta, precum și numeroase referințe citate în acestea, au comentat o gamă largă de potențiale sintetice.
În sinteza glicozidelor, componentele multi-zaharidice sunt combinate cu nucleofili, cum ar fi alcoolii, carbohidrații sau proteinele. Dacă este necesară o reacție selectivă cu una dintre grupările hidroxil ale unui carbohidrat, toate celelalte funcții trebuie protejate în prima etapă. În principiu, procesele enzimatice sau microbiene, datorită selectivității lor, pot înlocui etapele complexe de protecție chimică și deprotejare pentru a elimina selectiv glicozidele în anumite regiuni. Cu toate acestea, datorită istoriei îndelungate a glicozidelor alchilice, aplicarea enzimelor în sinteza glicozidelor nu a fost studiată și aplicată pe scară largă.
Datorită capacității sistemelor enzimatice adecvate și a costurilor ridicate de producție, sinteza enzimatică a alchilpoliglicozidelor nu este gata pentru a fi modernizată la nivel industrial, fiind preferate metodele chimice.
În 1870, MAcolley a raportat sinteza „acetoclorhidrozei” (1, figura 2) prin reacția dextrozei (glucozei) cu clorura de acetil, ceea ce a dus în cele din urmă la istoria rutelor de sinteză a glicozidelor.
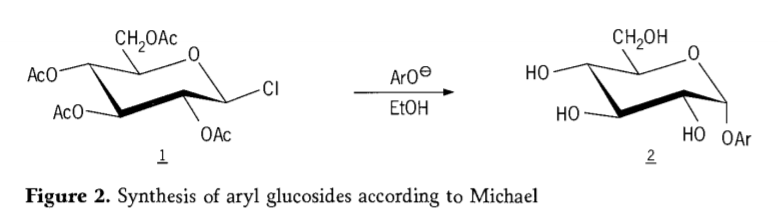
Halogenurile de tetra-O-acetilglucopiranozil (acetohaloglucozele) s-au dovedit ulterior a fi intermediari utili pentru sinteza stereoselectivă a glucozidelor alchilice pure. În 1879, Arthur Michael a reușit să prepare glicozide arilice cristalizabile, definite, din intermediari Colley și fenolați. (Aro-, Figura 2).
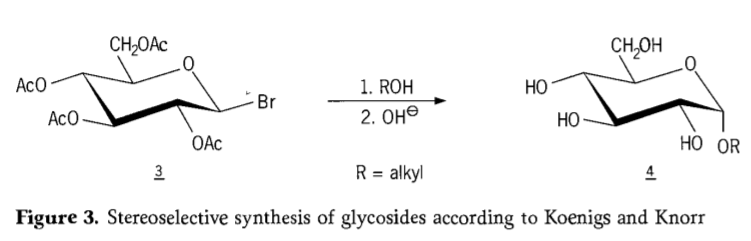
În 1901, sinteza lui Michael a condus la o gamă largă de carbohidrați și agliconi hidroxilici, când W. Koenigs și E. Knorr au introdus procesul lor îmbunătățit de glicozidare stereoselectivă (Figura 3). Reacția implică o substituție SN2 la carbonul anomeric și se desfășoară stereoselectiv cu inversarea configurației, producând, de exemplu, α-glucozida 4 din β-anomerul intermediarului aceobromoglucoză 3. Sinteza Koenigs-Knorr are loc în prezența promotorilor de argint sau mercur.
În 1893, Emil Fischer a propus o abordare fundamental diferită pentru sinteza alchilglucozidelor. Acest proces este acum bine cunoscut sub numele de „glicozidare Fischer” și cuprinde o reacție catalizată de acid a glicozelor cu alcooli. Orice relatare istorică ar trebui totuși să includă și prima încercare raportată a lui A. Gautier din 1874 de a converti dextroza cu etanol anhidru în prezența acidului clorhidric. Din cauza unei analize elementare înșelătoare, Gautier a crezut că a obținut o „diglucoză”. Fischer a demonstrat ulterior că „diglucoza” lui Gautier era de fapt în principal etilglucozidă (Figura 4).
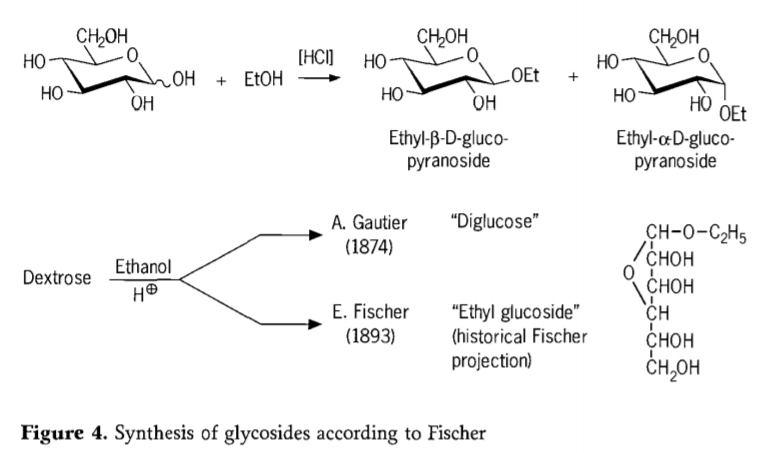
Fischer a definit corect structura etilglucozidei, așa cum se poate observa din formula furanozidică istorică propusă. De fapt, produșii de glicozidare Fischer sunt amestecuri complexe, în mare parte la echilibru, de α/β-anomeri și izomeri de piranozidă/furanozidă, care cuprind și oligomeri glicozidici legați aleatoriu.
Prin urmare, speciile moleculare individuale nu sunt ușor de izolat din amestecurile de reacție Fischer, ceea ce a reprezentat o problemă serioasă în trecut. După unele îmbunătățiri ale acestei metode de sinteză, Fischer a adoptat ulterior sinteza Koenigs-Knorr pentru investigațiile sale. Folosind acest proces, E. Fischer și B. Helferich au fost primii care au raportat sinteza unei glucozide alchilice cu lanț lung care prezintă proprietăți surfactante în 1911.
Încă din 1893, Fischer observase corect proprietățile esențiale ale glicozidelor alchilice, cum ar fi stabilitatea lor ridicată la oxidare și hidroliză, în special în medii puternic alcaline. Ambele caracteristici sunt valoroase pentru poliglicozidele alchilice în aplicațiile surfactanților.
Cercetările legate de reacția de glicozidare sunt încă în curs de desfășurare și în trecutul recent au fost dezvoltate mai multe rute interesante de obținere a glicozidelor. Unele dintre procedurile de sinteză a glicozidelor sunt rezumate în Figura 5.
În general, procesele de glicozidare chimică pot fi împărțite în procese care duc la echilibre oligomerice complexe în schimbul de glicozil catalizat de acid.
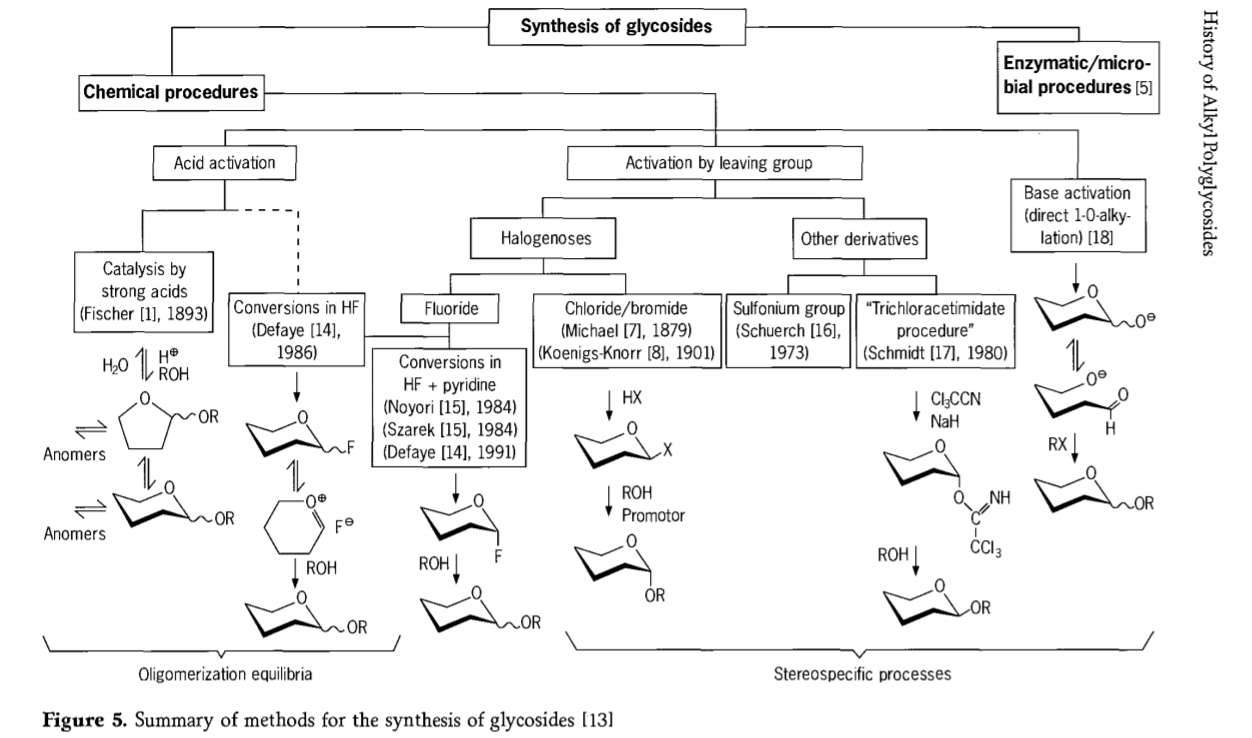
Reacții pe substraturi carbohidrați activate corespunzător (reacții glicozidice Fischer și reacții de fluorură de hidrogen (HF) cu molecule carbohidrați neprotejate) și reacții de substituție controlate cinetic, ireversibile și în principal stereotaxice. Un al doilea tip de procedură poate duce la formarea de specii individuale, mai degrabă decât la formarea de amestecuri complexe de reacții, în special atunci când este combinată cu tehnici de conservare a grupurilor. Carbohidrații pot lăsa grupări pe carbonul ectopic, cum ar fi atomii de halogen, sulfonilii sau grupările tricloracetimidat, sau pot fi activați de baze înainte de conversia în esteri triflați.
În cazul particular al glicozidărilor în fluorură de hidrogen sau în amestecuri de fluorură de hidrogen și piridină (poli[fluorură de hidrogen] de piridiniu), fluorurile de glicozil se formează in situ și sunt transformate ușor în glicozide, de exemplu cu alcooli. S-a demonstrat că fluorura de hidrogen este un mediu de reacție puternic activator, nedegradabil; se observă autocondensare la echilibru (oligomerizare) similară procesului Fischer, deși mecanismul de reacție este probabil diferit.
Glicozidele alchilice chimic pure sunt potrivite doar pentru aplicații foarte speciale. De exemplu, glicozidele alchilice au fost utilizate cu succes în cercetarea biochimică pentru cristalizarea proteinelor membranare, cum ar fi cristalizarea tridimensională a porinei și bacteriohodopsinei în prezența octil β-D-glucopiranozidei (experimente ulterioare bazate pe această lucrare au condus la Premiul Nobel pentru chimie pentru Deisenhofer, Huber și Michel în 1988).
Pe parcursul dezvoltării alchilpoliglicozidelor, metodele stereoselective au fost utilizate la scară de laborator pentru a sintetiza o varietate de substanțe model și pentru a studia proprietățile lor fizico-chimice. Datorită complexității lor, instabilității intermediarilor și cantității și naturii critice a deșeurilor de proces, sintezele de tip Koenigs-Knorr și alte tehnici de grupare protectoare ar crea probleme tehnice și economice semnificative. Procesele de tip Fischer sunt comparativ mai puțin complicate și mai ușor de realizat la scară comercială și, în consecință, reprezintă metoda preferată pentru producerea alchilpoliglicozidelor la scară largă.
Data publicării: 12 septembrie 2020





